2017年9月14日掲載
Vol.2ISO 15189 認定施設への One Point Information Vol.2
要求事項
4.14.6 リスクマネジメント
検査室は、患者の安全に影響を及ぼす作業プロセスならび検査結果の潜在的な欠陥の影響を評価しなければならない。認識されたリスクを低減、又は除去するためにプロセスを改良し、決定事項と講じた処置を文書化しなければならない。
解 説
ISO 31000(Risk management-Principles and guideline)に示されるリスクとは、「目的に対する不確かさの影響」であり、事象から生じる結果は好ましいものから、好ましくないものまで変動するとしていますが、臨床検査の側面では、リスクの結果は常に好ましくないものとの考えに基づき、4.14.6 リスクマネジメントの要求事項となっています。
ところで、ISO 15189規格4.2.1では、「QMSは品質方針及び品質目標,並びに利用者のニーズや要求事項を満たすために要求されるすべての プロセスの完全性を提供しなければならない。」としています。すなわち、多くのプロセスの組合せ(プロセスアプローチ)によって構築されたQMSが、『1つのまとまったシステム』として、各プロセスとの相乗効果を生みながら効果的に運用するためには、各々のプロセスの完全性が担保されることが重要となります。
臨床検査室のQMSでは、リスクマネジメントの材料にインシデントやアクシデントの報告書が用いられることが多々ありますが、個々のインシデントやアクシデントの処置は、上記の視点から考えると、各プロセス(機能)における欠陥(不適合)あるいはアクシデントを引き起こす潜在的な欠陥への対応であり、『品質マネジメントシステムにおけるトラブルシューティング』 と言えます。
臨床検査室のリスクマネジメントが、個々のトラブルシューティングに偏り、QMSを1つのまとまった統括的なシステムとしてリスクマネジメントを捉える観点が不明瞭となれば、リスクマネジメントは後ろ向きのシステム(対策)になりやすいと言えます。
FLS(Future Lab Session)は、4.12継続的改善の「検査前プロセス、検査プロセス、検査後プロセスを含む品質マネジメントシステムの有効性を継続的に改善しなければならない。改善活動は、リスクアセスメントをもとに最優先事項の領域で指揮されなければならない。」という要求事項からも4.14.6 リスクマネジメントの要求事項は、トラブルシューティングではなく、事象の傾向や頻度を含む継続的改善へのアプローチとして捉え、QMSを1つのまとまった統括的なシステムであるという視点で、「リスク特定☞リスク分析☞リスク評価」に系統的な解析を加え、リスク対策を未来志向的に検討しました。
理 論 編
ISO 15189規格ではどの様なプロセスからリスクの特定を行くべきか?要求事項は、「患者の安全に影響を及ぼす作業プロセス及び検査結果の潜在的な欠陥の影響を評価する」ことを求めていることから、4章より5章のプロセスが大筋でリスクの特定をする範囲であり、特に4.12継続的改善で「改善活動は、リスクアセスメントの・・・・」の前段にある文書、「検査前プロセス、検査プロセス、検査後プロセスを含むQMSの有効性を継続的に改善しなければならない」の流れから、5.4・5.5・5.7の範囲を中心にリスクの特定を進めて行くのが本筋であると言えます。
但し、上記に述べた「QMSを1つのまとまった統括的なシステムである」という視点から、これまでの5章のすべて(5.1~5.10)に関わる内部監査の指摘、アクシデントやインシデントの事例を「リスク分析の対象とするリスク」として特定します。
次にリスク分析とは、影響とその起こりやすさの双方を検討することから、以下のリスクマップ(図1)をベースに5章の各プロセスを分析します。また、リスクマップに示した各領域での対策は、基本的に「低減」「回避」「移転」「保有」「共有」の何れか、またはその組み合わせとなります。
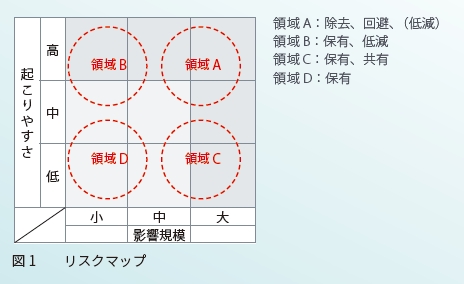
ISO 15189 における「影響規模」とは、要求事項の内容から ①患者の安全面から患者と直接・間接的に関わる作業プロセス ②検査過誤に繋がる作業プロセス以上の2点に関与する程度を影響度と定義することができます。そこで、まずこれまでの内部監査の指摘、アクシデントやインシデントの事例を5.1~5.10に分類します。次に各事象は①や②にどの程度、関与しているかを評価します。そして、「起こりやすさ」は発生回数頻度と理解すれば、内部監査の指摘、アクシデントやインシデントの事例を5.1~5.10の何れかに分類し、個々に積算した件数を発生頻度として使用します。
その分析結果を図1に展開し、5.1~5.10のグループが特徴ある領域を示すことができれば、発生した不適合に対し、該当する項番を付与することで、各々の事象に対する適切なリスク対策を行うための方向性を見出すことができます。
4.12 継続的改善には、「改善活動は、リスクアセスメントをもとに最優先事項の領域で指揮されなければならない」ことを要求しており、最優先事項とは、図1のA領域で発生する事象へのリスク対策を優先することになります。そして、4.10 是正処置 c)「不適合の再発防止を確実にするための是正処置の必要性の評価」、4.11 予防処置 c)「不適合の発生を予防するための処置の必要性の評価」が、この図1の領域を利用して効果的に行える可能性が出てきます。
実 践 編
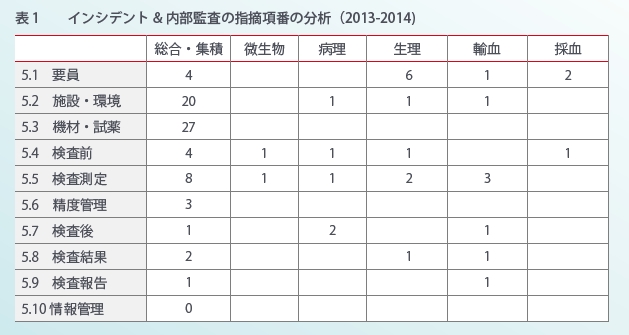
今回、この理論を基に具体的に分析を試みたFLSのA認定施設は、①500床以上、②特定機能病院、③認定範囲基幹項目1~6、非基幹項目 11~17、病理学的検査31,32④認定範囲の要員数約40人、⑤認定取得後、約3年が経過という状況です。2013年から2014年の2年間で5章に関するインシデント&内部監査の指摘事項(合計99件)を5.1~5.10に分類し、一覧表に纏めました。
ここで表1の“総合・集積”とは検体系を意味しています。
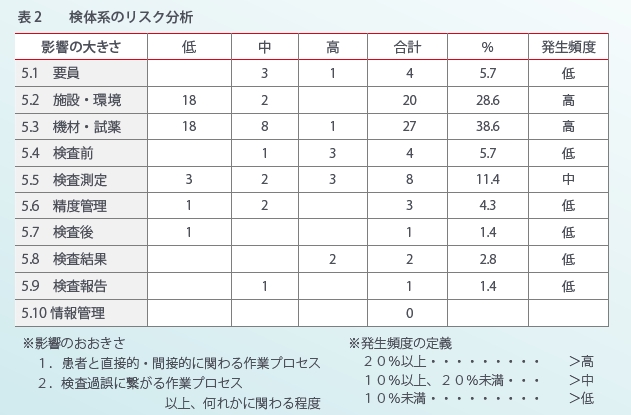
次に理論編から5.1~5.10のグループが特徴ある領域を示すことができるかを確認するため、今回集計でN数の多い検体系だけを抽出し、影響の大きさは理論編の①②に基づき、発生頻度は検体系全70 件に占める割合で定義し表2を作成しています。
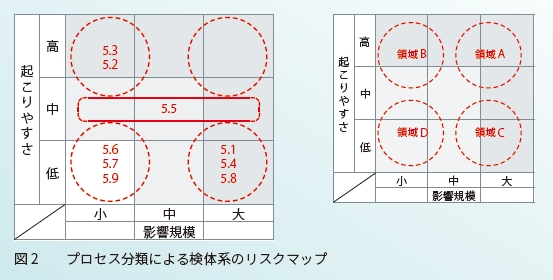
すなわち、検体系におけるA領域に存在する5章はなく、B領域(保有、低減)に5.3,5.2C 領域(保有・共有)に5.1,5.4,5.8 D 領域(保有)に5.6,5.7.5.9そして、特徴的なのは5.5で発生頻度は中レベルですが、影響度の範囲は広く様々な領域で存在し、影響度の程度は事象により異なることがわかりました。
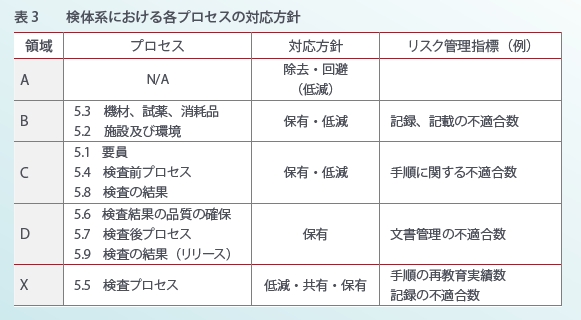
このリスクアセスメント(リスク特定+リスク分析+リスク評価)から、5.1~5.10の各プロセスに応じたリスクへの対応方針が明確となり、それに伴い1つの例としてリスクを監視する管理指標を見出すことができました。(表3)
ISO 9001:2015 では、2008 年版の予防処置の考えが反映されながら、6.計画に“6.1リスク及び機会への取組み” として 改訂されました。この6.1はQMSの計画段階で、計画どおりの結果を得るために事前に対応を講じておくべきリスク及び機会として何があるかを検討し、決定したリスク及び機会への取組みを計画の中に組み込んでおくことを求めており、QMS全体にリスク及び機会という概念を含ませる。すなわち、QMSに必要なプロセスにリスク及び機会への取組みを組み込むことで、プロセスアプローチに基づく運営管理を推進することを求めています。これは、上記の解説編で示した「QMSを1つのまとまった統括的なシステムであるという視点で、リスクマネジメントをQMS の継続的改善へのアプローチ」(未来 志向的な検討)であるという考えに一致しています。
すでにQMSを展開している臨床検査室は、5 章の各プロセスに紐付けられた手順書やSOPの定期的レビューの機会は存在しています。その際に各手順書に示された作業プロセスの潜在的な欠陥の有無を洗い出し、表3の対応方針に基づいてリスク管理指標を手順書の中に組み込み、そして継続的な監視を行う。これは4.12継続的改善で要求されている「適切な場合、改善活動のための行動計画を策定し、文書化し、実行しなければならない」という要求事項を具体化する1つの方法論と考えます。また、内部監査等による不適合に対する是正処置から予防処置への展開時には、5.1~5.10 の何れの不適合なのかが明確になるなら、表3の対応方針が改善活動を立案する指針ともなります。
引用文献:資料
1)Future Lab Session in OSAKA第2回 ブラッシュアップセミナー
2)ISO 15189:2012 英和対訳版(一般財団法人 日本規格協会 出版事業部)
3)ISO 9001:2015 新旧規格の対照と解説 著者 中篠武志・須田晋介 ( 一般財団法人 日本規格協会)
4)ISO 31000:2009 リスクマネジメント解説と適用ガイド編著リスクマネジメント規格活用検討会( 一般財団法人 日本規格協会)
監修:Future Lab Session in OSAKA世話人会
発行:ベックマン・コールター株式会社
- PDF版ダウンロードはこちら
- ダウンロード
これから先のページでは、医療関係者の方々を対象に医療機器・体外診断薬等の製品に関する情報を提供しております。当社製品を適正に使用していただくことを目的としており、一部の情報では専門的な用語を使用しております。
一般の方への情報提供を目的としたものではありませんので、ご了承ください。
医療関係者の方は、次のページへお進みください。
(お手数ですが、「進む」ボタンのクリックをお願いします)
