2019年12月11日掲載
Vol.5ISO 15189 認定施設への One Point Information Vol.5
要求事項
4.14.7 品質指標
検査室は, 検査前プロセス, 検査プロセス, 検査後プロセスの重要な側面全体の遂行能力を監視し, 評価するための品質指標を確立しなければならない。
解 説
上記の規格要求事項は4.14 評価及び監査にある項番です。3 用語及び定義の3.18 品質は、本来備わっている特性の集まりが要求事項を満たす程度としており、3.19 品質指標は、本来備わっている特性の集まりが要求事項を満たす程度の目安とあることから、4.14.7 品質指標は作り込まれた各プロセスが、適切に機能して期待した結果が得られているかを監視する「パフォーマンス指標」として、QMSの中で扱うことが重要です。
3.19 注記2) 品質指標は, 利用者のニーズ及び要求事項を組織が満たしている度合い, ならびにすべての業務プロセスの品質を測定することができる。(4.2.1 品質マネジメントシステム/一般要求事項 c)参照)と記載していることから、本来は検査前プロセス、検査プロセス、検査後プロセスだけではなく、他のプロセスにおいても品質指標を確立し、QMS全体のパフォーマンスを効率的で効果的に監視することが、QMSにおける理想的な品質指標の展開と言えます。その必要性は、4.2 品質マネジメントシステム 4.2.1 一般要求事項で読み取ることができます。「品質マネジメントシステムは, 品質方針及び品質目標, ならびに利用者のニーズや要求事項を満たすために要求されるすべてのプロセスの完全性を提供しなければならない。(☞ QMSのすべてのプロセスが期待した結果が得られている状態にあること)」とあります。従って、4.2.1 の要求事項を完全に満たすためには、QMSにおける必要なプロセスを明確化し、その相互作用を把握し、運用管理することと合わせて、一連のプロセスをシステムとして適用する“プロセスアプローチ”の考え方を理解する必要がありますが、この要求事項は、ISO 9001品質マネジメントシステムの概念を継承していると考えられます(4.2.1 一般要求事項 a)~f)参照)。
また、b)これらのプロセスの順序及び相互関係を明確にする。すなわち、QMSは各プロセスのネットワーク(☞1つのプロセスのアウトプットは、次のプロセスのインプットとなる)から組み上げられており、各プロセスのパフォーマンスを監視すると共に、1つのプロセスの変更が他のプロセスに及ぼす影響も監視しながら、QMSの全体最適を追究することが、プロセスの完全性を維持継続させることに繋がります。
4.14.7 品質指標 「検査室は, 利用者と協議して, 臨床のニーズを反映した個々の検査の所要時間を確立しなければならない。検査室は, 確立した所要時間を満たしていることを定期的に評価しなければならない。」とあります。これは、検査前プロセス、検査プロセス、検査後プロセスの一連のプロセス全体を1つの品質指標(TAT)で監視し、そのパフォーマンスが期待した結果通りに得られない場合は、個々のプロセスの品質指標のパフォーマンスを調査し、ボトルネックとなっているプロセスの監視を強化する、又は、改善策を講じるプロセスアプローチを行うことで、この一連のプロセスの全体最適を維持継続されることになります。
4.1.2.4 品質目標及び品質計画に関わって、品質目標の達成度の判定指標として、品質指標が組み込まれることがありますが、これは品質指標の二次的な利用方法であり、1つのプロセスのパフォーマンスが期待した結果が常に得られている状況において、意図的にパフォーマンスをさらに向上させることが、品質目標として設定する場合に品質指標が使われることがあります。しかし、これは、あくまで品質指標の側面を利用したものであると言えま。
理 論 編
臨床検査室のQMSに品質指標を組み込むことを検討してみます。4.14.7 品質指標の例に “受入不可サンプル数”とあり、これを「検査前プロセス」の品質指標として考えた場合、以下の幾つかある手順が適切に実施されていれば、受入不可サンプル数は基本的には期待した結果通りの件数以下に収まるはずです。
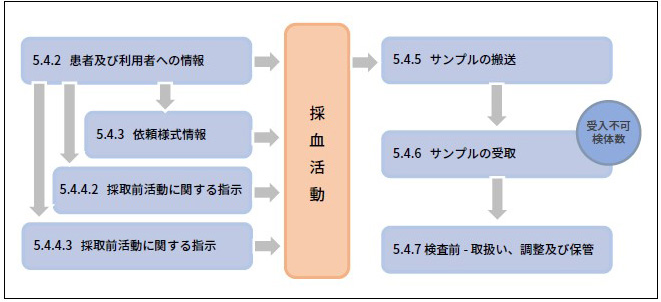
5.4 検査前プロセス
しかし、受入不可検体数だけが5.4 検査前プロセスに含まれるすべての手順が、適切に行われているかを反映したものではなく、適切性を監視するための最大公約数の品質指標として取り扱うべきです。そして、この「受付不可検体数」という品質指標が5.4 検査前プロセスを監視するにあたり、適切な指標として利用できているかをレビューする機会を4.15.2 レビューへのインプット “f)品質指標の利用”で要求しています。
また、4.14.7 品質指標では、「品質指標の監視プロセスは, 目標, 測定法, 解釈, 限界, 行動計画及び測定期間の確立を含む計画でなければならない。」としています。
<表1> (例) 品質指標の受入不可検体数の計画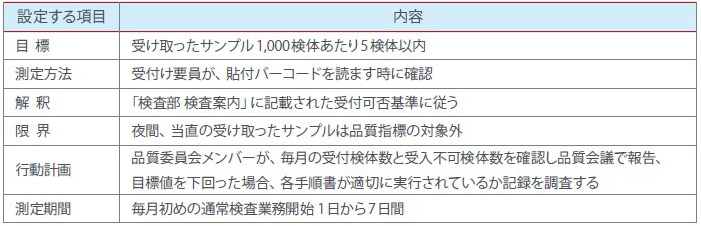
また、「指標は, 適切性が継続されていることを確実にするために, 定期的にレビューされなければならない。」とあり、検査前プロセス、検査プロセス、検査後プロセスは、日常の検査業務で展開されているため、品質指標のパフォーマンスは月単位の間隔でレビューを行い、目標(プロセスの機能に期待した結果)を下回った場合には、プロセスを構成する手順や規定及び記録を確認し、改善策を講じる必要があります。
実 践 編
理論編での要求事項を念頭に、今回、生化学検査での各プロセスにおける品質指標の設定を行った。
1. 検査前プロセスにおける品質指標
検討方法
・実際の未分注の親検体と子検体の搬出画像
(未分注でない検体は親検体のみ搬出される)

分析・検証結果
1ヶ月間未分注の結果を検討し、平均の未分注率から仮の品質指標を設定後、さらに検討を継続し、2ヶ月間の集計結果が若干想定の未分注率より高かったため、検査部の外来採血室の採血量遵守を啓蒙し、軽減を図ることとした。さらに詳しく未分注率の傾向を確認すると、午後からの詰まりエラーの頻度が多発していた。その原因は、検体投入スタッフが新人であり、凝血を確認せずに搬送投入していることが判明したため、再教育し、翌月の詰まりエラーを確認することとした。翌月の午後からの詰まりエラーの頻度が減少したため、この未分注率のデータを用いて検査前プロセスの品質指標の設定を行った。
2. 検査プロセスにおける品質指標
検討方法
分析・検証結果
数ヶ月間の検討後、メンテナンス等の作業を行った後のコントロール測定は、トラブル等の偶発誤差以外の原因を多く含むため、0.3%以内にすることは困難であると判断し、品質指標の検討方法の見直しを行い、『業務中のコントロールの測定で搬送内自動測定のみの偶発誤差が0.3%を超えた結果を監視する』に変更した。
その後、1ヶ月の搬送内での業務中のコントロール自動測定の偶発誤差が、0.3%を超えた項目数は、25種類あり、この結果を検査プロセスの品質指標とした。
生化学検査の汎用自動機器でコントロールを測定した場合に±3SDを外れる頻度は、項目により傾向が見られることから、これらをもとにさらに検討を続け、項目ごとの品質指標の決定を行い、より精度の高い品質指標の検討を続けることとした。
3. 検査後プロセスにおける品質指標
検討方法
分析・検証結果
再検率が高値であったP型アミラーゼのリアルタイム精度管理に、前回値チェックのロジックを追加したシミュレーションを行った。再検率は、少し改善が見られたが大きくは変動していないため、4ヶ月の検討データにシミュレーションのデータを考慮し、検査後プロセスの品質指標の設定を行っ。
4. ISO 15189の導入後の品質指標の分析・検証におけるPDCAサイクル
「方針・目標・計画の立案(Plan)」・「実行(Do)」・「効果の確認(Check)」・「処置・改善(Action)」を行い、検査室をよりよくするための継続的改善の体制(PDCAサイクル)を整えなければならない。そのために各プロセスの品質指標を決定し、品質を確保する。また、改善が必要な品質指標においては、目標の設定・品質計画の実行を行い、PDCAサイクルを回すことが品質の確保・向上に重要であると思われた。
5. まとめ
当院は現在、ISO15189の初回審査、第1回サーベイランスを終了し、QMSの維持活動は、スタートしたばかりで、これから要求事項の理解を深めていくことは重要な課題である。認定取得で満足してしまっていた時期に、この品質指標の設定を行い、毎年度の目標につなげていくことが、QMSの維持活動の継続につながること、的確な品質指標の設定を行うことで、安定した品質の検査結果報告が、監視可能であることを実感した。
今回の品質指標の設定は、まだ各プロセスの一部であるが、さらに別の要素も含めて詳しく分析し、設定していくことにより有効な品質の監視が可能であると思われる。
さらに、すべてのプロセスにおいて品質指標を探求し、それがインプット・アウトプットでプロセス連鎖としてつながり、臨床検査の品質の向上となっていくことが重要であるとも思われた。
すなわち、品質指標を設定し継続的な改善体制(PDCAサイクル)を構築することで、検査結果の信頼性の向上やリスクの最小化、コスト削減などの効果となることが期待できる。
監修:Future Lab Session in OSAKA 世話人会
発行:ベックマン・コールター株式会社
- PDF版ダウンロードはこちら
- ダウンロード
これから先のページでは、医療関係者の方々を対象に医療機器・体外診断薬等の製品に関する情報を提供しております。当社製品を適正に使用していただくことを目的としており、一部の情報では専門的な用語を使用しております。
一般の方への情報提供を目的としたものではありませんので、ご了承ください。
医療関係者の方は、次のページへお進みください。
(お手数ですが、「進む」ボタンのクリックをお願いします)
